Ce cours complète le MOOC « Thermodynamique : fondements » qui vous permettra de mettre en application les concepts fondamentaux de la thermodynamique. Pour atteindre cet objectif, le Professeur J.-Ph. Ansermet de l’Ecole Polytechnique Fédérale de Lausanne s’est entouré d’experts et de spécialistes des différents domaines d’application provenant de diverses institutions partenaires du réseau RESCIF. Vous pourrez ainsi voir l’usage de la thermodynamique en chimie, en ingénierie et en physique.


Thermodynamique : applications
Taught in French
6,006 already enrolled
(10 reviews)
Details to know

Add to your LinkedIn profile
30 quizzes
See how employees at top companies are mastering in-demand skills


Earn a career certificate
Add this credential to your LinkedIn profile, resume, or CV
Share it on social media and in your performance review

There are 9 modules in this course
Dans ce chapitre, le professeur Paul Ekam de l'Institut Polytechnique de Yaoundé au Cameroun présente la manière dont on modélise les échanges infinitésimaux de chaleur. Ceux-ci sont fonction de plusieurs variables d'état reliées par des coefficients appelés coefficients calorimétriques. Les potentiels thermodynamiques permettent ensuite de déterminer des relations entre ces coefficients. Finalement ces coefficients sont appliqués dans le cas d'un gaz parfait pour calculer les échanges de travail et de chaleur pour les processus standard (isotherme, adiabatique et isochore).
What's included
6 videos3 readings4 quizzes
Dans ce chapitre, le docteur Marthe Boyomo de l'Institut Polytechnique de Yaoundé au Cameroun présente les éléments de base de la théorie des transitions de phase, c'est-à-dire des variations abruptes de l'état de la matière. La première partie traite de la stabilité de ces états. La deuxième partie traite des transitions dites de premier ordre. Dans la troisième partie, ceci est illustré par l'exemple de la transition liquide-vapeur en utilisant le modèle de van der Walls.
What's included
4 videos3 quizzes
Dans ce chapitre, le docteur Théophile Mbang de l'Institut Polytechnique de Yaoundé au Cameroun applique les concepts de la thermodynamique pour modéliser la dynamique des réactions chimiques. Il introduit l'avancement d'une réaction chimique et définit l'enthalpie et l'énergie libre de Gibbs d'une réaction chimique. Il discute aussi la loi de Hess et la loi d'action de masse.
What's included
6 videos4 quizzes
Dans ce chapitre le professeur M. Graetzel de l'Ecole Polytechnique Fédérale de Lausanne en Suisse applique les concepts de la thermodynamique à l'électrochimie. Les outils de base de la thermodynamique permettent de modéliser les fonctionnement des batteries, ainsi que celui des piles à combustibles. Le cas d'une pile à concentration est abordé en exercice. La généralisation du potentiel chimique en électrochimie est le potentiel électrochimique qui rend notamment comptes des interactions électrostatiques entre des ions.
What's included
5 videos3 quizzes
Dans ce chapitre le professeur André Talla de l'Institut Polytechnique de Yaoundé au Cameroun applique les concepts de la thermodynamique à des fluides. Il décrit en particulier des processus isothermes, adiabatiques, isochores et isobares. En considérant un cycle thermodynamique ditherme (constitué de deux isothermes) il définit la notion de rendement et celle d'efficacité.
What's included
5 videos4 quizzes
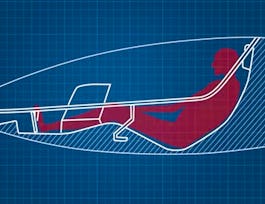
Dans ce chapitre, le professeur Etienne Robert de l'École Polytechnique de Montréal au Canada discute les applications techniques des cycles thermodynamiques. Il explique le fonctionnement du moteur à combustion, des turbine à gaz et des pompes thermiques.
What's included
5 videos4 quizzes
Dans ce chapitre le Docteur Marwan Brouche et le Docteur Chantal Maatouk de l'université Saint-Josèphe à Beyrouth au Liban traitent des transferts de chaleur par convection, conduction et radiation. Ils discutent notamment l'équation de la chaleur.
What's included
7 videos2 quizzes
Dans ce chapitre, le professeur Miltiadis Papalexandris de l'Université Catholique de Louvain en Belgique développe une description locale de la thermodynamique où les systèmes locaux sont à l’équilibre. Cela lui permet de définir les champs intensifs "température", "pression" et "potentiel thermodynamique". En suivant cette approche, il détermine notamment les équations qui localement gouvernent la thermostatique, la thermodynamique des processus réversibles et celle des processus irréversibles.
What's included
3 videos3 quizzes
Dans ce chapitre, le professeur Miltiadis Papalexandris de l'Université Catholique de Louvain en Belgique applique la thermodynamique des milieux continus pour modéliser les processus irréversibles. Ces processus sont décrits par des relations linéaires entre les courants généralisés et les forces généralisées qui décrivent des lois et des effets physiques. Comme exemple, il présente entre autres les lois d’Ohm, de Fick et de Fourier, et les effets Hall, Seebeck et Joule.
What's included
3 videos3 quizzes
Instructors



Offered by
Recommended if you're interested in Physics and Astronomy
École Polytechnique Fédérale de Lausanne

Coursera Project Network
Coursera Project Network
Why people choose Coursera for their career





Open new doors with Coursera Plus
Unlimited access to 7,000+ world-class courses, hands-on projects, and job-ready certificate programs - all included in your subscription
Advance your career with an online degree
Earn a degree from world-class universities - 100% online
Join over 3,400 global companies that choose Coursera for Business
Upskill your employees to excel in the digital economy
Frequently asked questions
Access to lectures and assignments depends on your type of enrollment. If you take a course in audit mode, you will be able to see most course materials for free. To access graded assignments and to earn a Certificate, you will need to purchase the Certificate experience, during or after your audit. If you don't see the audit option:
The course may not offer an audit option. You can try a Free Trial instead, or apply for Financial Aid.
The course may offer 'Full Course, No Certificate' instead. This option lets you see all course materials, submit required assessments, and get a final grade. This also means that you will not be able to purchase a Certificate experience.
When you purchase a Certificate you get access to all course materials, including graded assignments. Upon completing the course, your electronic Certificate will be added to your Accomplishments page - from there, you can print your Certificate or add it to your LinkedIn profile. If you only want to read and view the course content, you can audit the course for free.
You will be eligible for a full refund until two weeks after your payment date, or (for courses that have just launched) until two weeks after the first session of the course begins, whichever is later. You cannot receive a refund once you’ve earned a Course Certificate, even if you complete the course within the two-week refund period. See our full refund policy.